Klimaschutz aus dem Reagenzglas
Es wäre ein dreifacher Gewinn – fürs Klima, für die Rohstoffressourcen und für die chemische Industrie: Mit ihrer Arbeit wollen Wissenschaftlerinnen und Wissenschaftler des Fritz-Haber-Instituts der Max-Planck-Gesellschaft in Berlin die Basis schaffen, um aus dem Methan, das bei der Erdölförderung bislang abgefackelt wird, nützliche chemische Produkte wie etwa Kunststoffe zu gewinnen. Denn sie gehen der Frage nach, wie ein Katalysator beschaffen sein muss, der das Methan effizienter, als es derzeit möglich ist, in Ethen umwandelt. Einen wegweisenden Hinweis haben sie nun gefunden, den das FHI am 30.10.2020 auf seiner Internetseite publizierte.

Leuna – Total-Raffinerie mit 140m hoher Gasfackel – Foto © Gerhard Hofmann für Solarify
Rund 140 Milliarden Kubikmeter Methan, das bei der weltweiten Erdölförderung entweicht, werden jährlich abgefackelt – deutlich mehr als die schätzungsweise 90 Milliarden Kubikmeter Erdgas, die Deutschland im Jahr 2019 verbraucht hat. Das heizt nicht nur den Klimawandel an, sondern verschwendet auch einen fossilen Rohstoff, der irgendwann zur Neige gehen wird. Das gasförmige Methan lässt sich bislang jedoch nicht mit vertretbarem Aufwand nutzen: Für die an den einzelnen Erdölförderstätten anfallenden Mengen Pipelines oder Anlagen zur Verflüssigung zu bauen, rentiert sich nicht. Lohnen würde sich der Transport erst, wenn man das Methan auf ökonomische Weise in Stoffe umwandeln könnte, die für die chemische Industrie einen großen Nutzen haben. Eine solche Verbindung ist Ethen, der Ausgangsstoff des Allerweltskunststoffs Polyethylen und vieler weiterer Produkte der chemischen Industrie, die bislang fast ausschließlich aus Erdöl hergestellt werden. Der chemische Prozess, der Methan direkt in Ethen verwandelt, läuft bislang aber nur bei hohen Temperaturen. „Das kostet nicht nur viel Energie, sondern führt auch dazu, dass ein großer Anteil des Methans zum unerwünschten Nebenprodukt CO2 verbrennt“, sagt Annette Trunschke, Forschungsgruppenleiterin am Fritz-Haber-Institut der Max-Planck-Gesellschaft. „Das ist also noch nicht sinnvoll“.
Natrium ist der essenzielle Bestandteil
Die Chemikerin und ihr Team wollen dazu beitragen, das zu ändern. Deshalb haben sie sich die entscheidende Komponente des Prozesses vorgenommen, den Katalysator aus Natrium, Mangan, Wolfram und Silicium, der die chemische Umwandlung von Methan in Ethen erst ermöglicht – wenn auch bislang nur bei 700 Grad Celsius. Um Katalysatoren zu entwickeln, die bei niedrigeren Temperaturen, sprich mit weniger Energieaufwand arbeiten, und dann möglichst auch nur die Bildung der gewünschten Produkte fördern, müssen Chemiker erst einmal wissen, worauf es bei einem Katalysator für diese Reaktion ankommt. Den Untersuchungen von Trunschkes Gruppe zufolge ist dieser essenzielle Bestandteil das Natrium.
„Bislang gab es mehrere Theorien, welches Element im Katalysator entscheidend ist, um Methan in Ethen umzuwandeln“, sagt Annette Trunschke. „Dass ausgerechnet Natrium der wichtige Bestandteil ist, war nicht unbedingt zu erwarten, denn eigentlich sollte es bei den hohen Temperaturen der Reaktion allmählich verdampfen.“ Die Untersuchungen des Max-Planck-Teams zeigen jedoch etwas anderes: Bei der hohen Temperatur wird das Alkalimetall in das katalytisch wirksame Natriumoxid umgewandelt. Das Oxid wird durch eine enge Wechselwirkung mit den anderen Bestandteilen des Katalysators nur kurzzeitig und in kleinsten Mengen freigegeben und so daran gehindert zu verdampfen. „Damit wird klar, dass die anderen Bestandteile des Katalysators nur benötigt werden, um während der Arbeit die aktive Form des Katalysators freizusetzen und zu stabilisieren“, so Trunschke.
Live-Schalte zum arbeitenden Katalysator
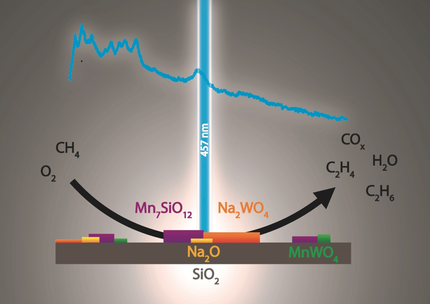
Geben und Nehmen: Die Operando-Raman-Spektroskopie in Kombination mit In-situ-RFA und thermischer Analyse wurde angewandt, um einen Mn-Na2WO4/SiO2-Katalysator bei der oxidativen Kopplung von Methan zu untersuchen. Das Schmelzen der Na2WO4- und Mn7SiO12-MnWO4-Redox-Chemie erfolgt gleichzeitig, wodurch die transiente Freisetzung und Lagerung aktiver Natriumoxid-Spezies ermöglicht wird. Die Kopplung dieser Prozesse ist wesentlich, um eine Deaktivierung des Katalysators zu vermeiden – Bild © FHI/onlinelibrary.wiley.com
Zu diesen Erkenntnissen sind die Forschenden gelangt, weil sie dem Katalysator erstmals live bei der Arbeit zuschauten: In einer eigens entwickelten Apparatur analysierten sie mithilfe der Raman-Spektroskopie, welche Substanzen am Katalysator entstehen, während die Ausgangsstoffe der Reaktion über ihn strömten. Maximilian Werny, der die Experimente in seiner Masterarbeit gemacht hat: „Bislang wurden die Katalysatoren nur vor und nach der Katalyse untersucht. Analysen mittels Raman-Spektroskopie bei hohen Temperaturen gibt es bislang nur am nicht arbeitenden Katalysator. Wir haben in der Raman-spektroskopischen Untersuchung jetzt erstmals beobachtet, wie die Produkte entstehen.“
Sowohl die Möglichkeit, eine Liveschalte zur Umwandlung von Methan in Ethen einzurichten, als auch die Erkenntnisse über den Katalysator aus Natrium, Mangan, Wolfram und Silicium könnten Chemikern nun helfen, chemische Vermittler zu entwickeln, die bei niedrigeren Temperaturen arbeiten und damit auch gezielter nur die gewünschten, nützlichen Produkte und kein CO2 erzeugen. Ein Ansatz könnte dabei sein, Natrium durch andere Alkalimetalle zu ersetzen und zu testen, ob die entsprechenden Katalysatoren bei niedrigeren Temperaturen Ethen erzeugen. „Dann benötigt man wahrscheinlich andere Komponenten, die das Metall festhalten“, sagt Annette Trunschke. Wie Kandidaten für alternative Katalysatoren arbeiten, könnten sie und ihr Team dann wieder live verfolgen. So dürften Chemiker Schritt für Schritt zu einem Katalysator gelangen, mit dem sich bei der Erdölförderung die Verschwendung von Methan vermeiden ließe und zumindest ein kleiner Beitrag zum Klimaschutz möglich würde.
->Quellen: