Chemikern gelingt Synthese eines kationischen, niederwertigen Aluminium-Komplexsalzes via Metathese
Durch Zusatz von Liganden, wie etwa beim Dimethylaminopyridin, wird die dimere Struktur des Kations aufgebrochen und das einsame Aluminiumatom zeigt seinen starken Akzeptorcharakter – so eine Medienmitteilung der Albert-Ludwigs-Uni Freiburg vom 12.08.2022.
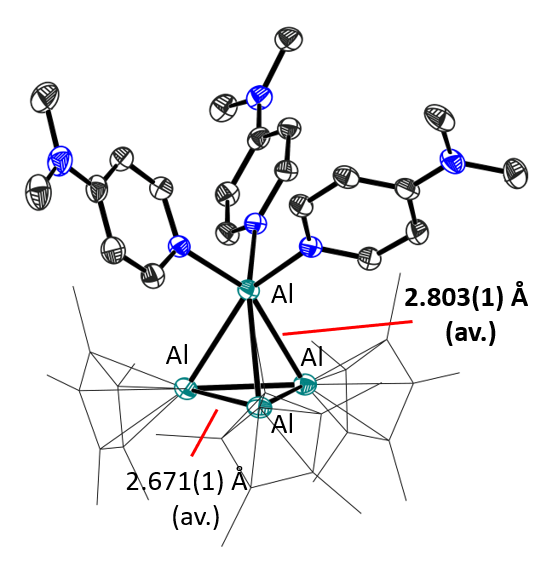
Zusatz von Liganden, hier Dimethylaminopyridin, bricht dimere Struktur des Kations auf – das einsame Aluminiumatom zeigt starken Akzeptorcharakter – Abbildung © von der Forschungsgruppe zur Verfügung gestellt, AG Krossing, uni-freiburg.de
Den Chemikern Philipp Dabringhaus, Julie Willrett und Prof. Ingo Krossing vom Institut für Anorganische und Analytische Chemie der Universität Freiburg ist die Synthese des niedervalenten kationischen Aluminiumkomplexes [Al(AlCp*)3]+ durch eine Metathese-Reaktion gelungen. Ihre Forschungsarbeit stellt das Team im Journal Nature Chemistry vor.
„In der Chemie sind kationische niedervalente Aluminiumverbindungen aufgrund ihrer potenziellen übergangsmetallähnlichen ambiphilen Reaktivität sehr begehrt. Zahlreiche bisherige Versuche zur Synthese von kationischen, niedervalenten Aluminiumverbindungen durch oxidative oder reduktive Verfahren blieben aber weitgehend erfolglos“, erklärt Krossing. Bisher gebe es nur ein Beispiel für eine kationische, niedervalente Aluminiumverbindung, die jedoch nicht durch eine rationale Synthese hergestellt werden kann. „Wir zeigen jetzt, dass es mit Metathese doch einen unerwartet leichten Zugang zu niederwertigen Aluminiumkomplexen gibt“, so Krossing. Bei der Metathese werden Teilstrukturen zwischen den Reaktionspartnern einfach ausgetauscht.
Aluminium als günstigere Alternative für die Katalyse
Die Freiburger Chemiker stellten das Salz [Al(AlCp*)3]+[Al(OC{CF3)3}4]– aus dem Schnöckel-Tetramer (AlCp*)4 her, in dem Aluminium bereits in der Oxidationsstufe +1 vorliegt. Das (AlCp*)4 reagierte mit Li[Al{OC(CF3)3}4] und das Reaktionsgemisch färbte sich sofort von gelb nach rot. Bei der Kristallisation der Reaktionsmischung erhielten die Wissenschaftler*innen das [Al(AlCp*)3]+[Al(OC{CF3)3}4]–-Salz als dunkelviolette Kristalle. „Röntgenographische, UV-spektrometrische und rechnerische Untersuchungen zeigen das Vorliegen der dimeren Struktur sowohl im festen Zustand als auch in Lösung bei hoher Konzentration und niedriger Temperatur an, bei niedriger Konzentration und Raumtemperatur bildet sich jedoch das Monomer. Dies weist klar auf eine ambiphile Reaktivität des Kations hin“, so Dabringhaus.
„Folglich kann dieses Salz potenziell als Baustein für ein [:Al(L)3]+-Salz verwendet werden, das aufgrund seines kationischen Charakters in der Lage sein könnte, reversible oxidative Additionen und reduktive Eliminierungen von kleinen Molekülen durchzuführen“, erklärt Krossing. „Damit sind wir einen Schritt näher an unserem Fernziel, die Katalyse – die momentan mit teuren und seltenen Übergangsmetallen gemacht wird – langfristig mit Aluminium hinzubekommen. Aluminium ist das zweihäufigste Element in der Erdkruste und dazu prinzipiell in der Lage, wie unsere Arbeit zeigt. Aber bis unsere Forschung dazu Anwendung findet, dauert es wohl leider noch mindestens 20 Jahre.“
Faktenübersicht:
- Prof. Dr. Ingo Krossing leitet die Professur für Molekül- und Koordinationschemie am Institut für Anorganische und Analytische Chemie der Universität Freiburg und ist Mitglied des Exzellenzclusters Living, Adaptive and Energy-autonomous Materials Systems (livMatS).
- Krossing erhält für sein Projekt „InnoChem – Innocent Deelectronation Chemistry“, bei dem er zu einer allgemeingültigen Redox-Skala forscht, einen Advanced Grant des Europäischen Forschungsrats (ERC).
- Im Jahr 2018 wurde Krossing in die Heidelberger Akademie der Wissenschaften, 2020 in die Nationale Akademie der Wissenschaften Leopoldina aufgenommen.
- Krossing Forschungsschwerpunkte liegen bei: schwach koordinierenden Anionen, reaktiven Kationen, Katalyse zur Energiekonversion, vereinheitlichten Aziditäts- und Redox-Skalen sowie Batterie-Elektrolyten und -Materialien. Mehr zur Forschung von Ingo Krossing.
->Quelle und weitere Informationen:
- kommunikation.uni-freiburg.de/pm/2022/wichtiger-meilenstein-auf-dem-weg-zur-uebergangsmetall-katalyse-mit-aluminium
- chemistrycommunity.nature.com/expanding-the-field-of-low-valent-main-group-cations-to-aluminium
- Zum „Behind the Paper“-Artikel auf der Webseite von Nature Chemistry
- Originalpublikation: Dabringhaus, P., Willrett, J., Krossing, I. (2022): Synthesis of a low-valent Al4+ cluster cation salt. Nature Chemistry. DOI: 10.1038/s41557-022-01000-4